Po desetiletí sloužily léky na bázi protilátek jako základ moderní medicíny. Jejich superschopnost spočívá v jejich přesnosti : tyto proteiny jsou navrženy tak, aby rozpoznaly a navázaly se na specifické struktury na povrchu virů, bakterií nebo infikovaných buněk. Tuto přesnost však vždy provázelo vážné omezení – protilátky jsou v podstatě „externí“ nástroje. Mohou hlídkovat v krevním řečišti a ulpívat na povrchu buněk, ale historicky nedokázali proniknout buněčnou membránou a bojovat s hrozbami, které se v nich skrývají.
Nyní se tato bariéra začíná hroutit. Prostřednictvím kombinace proteinového inženýrství a umělé inteligence vědci našli způsob, jak nasměrovat cílenou sílu protilátek uvnitř buňky.
Problém: Proč jsou buňky nepřátelské vůči protilátkám
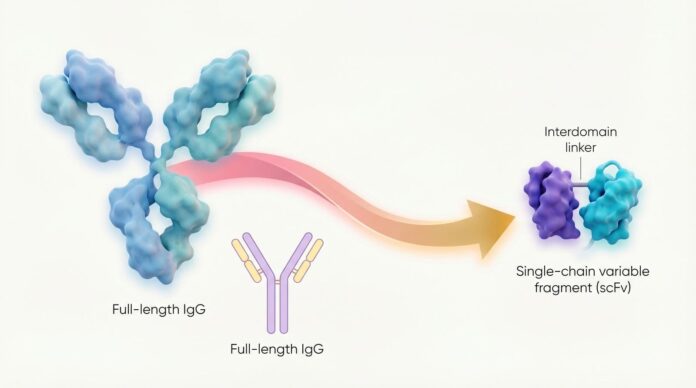
Abychom pochopili, proč se jedná o průlom, musíme pochopit, proč předchozí pokusy selhaly. Přestože se výzkumníci dlouho pokoušeli “zmenšit” protilátky na fragmenty, které by teoreticky mohly vklouznout do buněk, tyto fragmenty jen zřídka přežijí proces translokace.
Vnitřní prostředí buňky je chemicky odlišné od krevního řečiště. Hlavní překážkou je elektrický náboj. Standardní fragmenty protilátek mají často nábojový profil, který po zavedení do buňky má následující účinky:
– Agregace: fragmenty se slepí do zbytečných hrudek;
– Nesprávné skládání: ztrácejí svůj funkční tvar;
– Degradace: jsou zničeni dříve, než dosáhnou svého cíle.
Stručně řečeno, stejný mechanismus, který je činí účinnými mimo buňku, je činí uvnitř buňky nestabilními.
Řešení: Redesign s AI
Nový výzkum představil modulární platformu pro řešení této krize stability. Namísto snahy vnutit tradiční protilátky do buněk je výzkumníci od základu předělávají, aby mohly úspěšně fungovat v intracelulárním prostředí.
Zaměřením se na úpravu distribuce náboje ve vazebné části protilátky vědci úspěšně vytvořili více než 600 stabilních intracelulárních fragmentů protilátek.
Jak tento proces funguje:
- Zachování cíle: Přepracování se zaměřuje na jak se protilátka chová uvnitř buňky, spíše než na na co se váže. To zajišťuje, že lék stále rozpozná svůj specifický cíl.
- Integrace AI: Umělá inteligence se používá k modelování a úpravě proteinových struktur, což umožňuje rychle převést existující protilátky na verze „připravené pro buňky“.
- Škálovatelnost: Protože je modulární, lze jej aplikovat na stovky existujících protilátek a vytvořit tak obrovskou knihovnu nových terapeutických nástrojů.
Záchranné lano pro neurodegenerativní onemocnění
Nejhlubší důsledky této technologie spočívají v léčbě neurodegenerativních onemocnění.
Stavy jako Alzheimerova, Parkinsonova, Huntingtonova a amyotrofická laterální skleróza jsou způsobeny běžným destruktivním mechanismem: akumulací toxických, chybně poskládaných proteinů v mozkových buňkách. Protože tyto „molekulární motory“ nemoci jsou skryty za buněčnou membránou, tradiční protilátky jsou proti nim bezmocné.
S tímto novým přístupem bude terapie schopna:
– Zásah přesně do cíle: přímý kontakt se škodlivými proteinovými agregáty přesně v místě poškození;
– Zachování vysoké selektivity: odliší zdravé proteiny od nemocných, špatně poskládaných verzí, čímž se minimalizují vedlejší účinky;
– Použijte přenos genu: Budoucí léčba může využívat genovou technologii k indukci vlastních buněk pacienta k produkci těchto modifikovaných fragmentů protilátek v těle.
Globální dopad
Ačkoli je neurodegenerace oblastí s nejvyšší prioritou, potenciální aplikace platformy intracelulárních protilátek jsou obrovské. Nakonec může být tato technologie přizpůsobena pro boj s onkologickými onemocněními, zánětlivými poruchami a vzácnými genetickými stavy, kde je mechanismus vývoje onemocnění lokalizován v buňce.
Tento posun představuje zásadní změnu v biologické strategii: přechod od léčby symptomů na buněčném povrchu k zacílení na molekulární ovladače v srdci nemoci.
Závěr
Překonáním chemických bariér buněčného prostředí pomocí inženýrství řízeného umělou inteligencí otevřeli vědci nový rozměr ve vývoji léků. Tento průlom transformuje protilátky z externích sentinelů na interní přesné nástroje, které nabízejí naději na léčbu některých z nejnáročnějších a nejničivějších nemocí, které medicína zná.