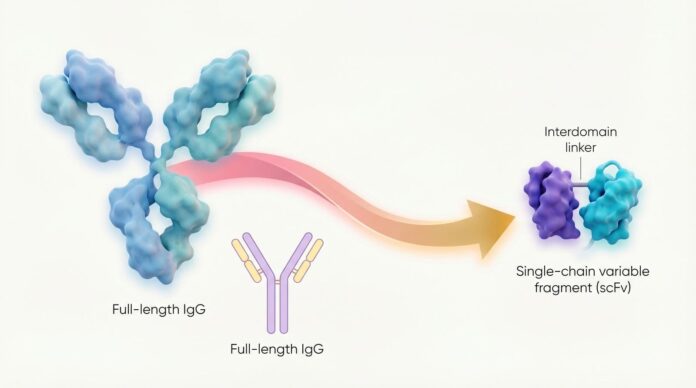
На протяжении десятилетий препараты на основе антител служили фундаментом современной медицины. Их суперсила заключается в точности : эти белки спроектированы так, чтобы распознавать и связываться со специфическими структурами на поверхности вирусов, бактерий или пораженных клеток. Однако эта точность всегда сопровождалась серьезным ограничением — антитела, по сути, являются «внешними» инструментами. Они могут патрулировать кровоток и цепляться за поверхность клетки, но исторически они были не способны проникать сквозь клеточную мембрану, чтобы бороться с угрозами, скрывающимися внутри.
Теперь этот барьер начинает рушиться. Благодаря сочетанию белковой инженерии и искусственного интеллекта ученые нашли способ направить целевую мощь антител внутрь клетки.
Проблема: почему клетки враждебны к антителам
Чтобы понять, почему это прорыв, нужно разобраться, почему предыдущие попытки не увенчались успехом. Хотя исследователи давно пытались «уменьшить» антитела до фрагментов, которые теоретически могли бы проскользнуть в клетку, эти фрагменты редко выживали в процессе перемещения.
Внутренняя среда клетки химически отличается от кровотока. Основным препятствием является электрический заряд. Стандартные фрагменты антител часто имеют такой профиль заряда, который при попадании внутрь клетки приводит к следующим последствиям:
— Агрегация: фрагменты слипаются в бесполезные комки;
— Неправильное сворачивание: они теряют свою функциональную форму;
— Деградация: они разрушаются до того, как достигнут цели.
Короче говоря, тот самый механизм, который делает их эффективными снаружи клетки, делает их нестабильными внутри неё.
Решение: редизайн с помощью ИИ
Новое исследование представило модульную платформу для решения этого кризиса стабильности. Вместо того чтобы пытаться насильно загнать традиционные антитела в клетки, исследователи перепроектируют их с нуля, чтобы они могли успешно функционировать вintracellular (внутриклеточной) среде.
Сосредоточившись на корректировке распределения заряда в связывающей части антитела, ученые успешно создали более 600 стабильных внутриклеточных фрагментов антител.
Как работает этот процесс:
- Сохранение мишени: Редизайн фокусируется на том, как антитело ведет себя внутри клетки, а не на том, с чем оно связывается. Это гарантирует, что препарат по-прежнему будет распознавать свою специфическую цель.
- Интеграция ИИ: Искусственный интеллект используется для моделирования и модификации белковых структур, что позволяет быстро превращать существующие антитела в версии, «готовые к работе внутри клетки».
- Масштабируемость: Поскольку это модульная структура, её можно применить к сотням существующих антител, создав огромную библиотеку новых терапевтических инструментов.
Спасательный круг для лечения нейродегенеративных заболеваний
Самые глубокие последствия этой технологии лежат в области лечения нейродегенеративных заболеваний.
Такие состояния, как болезни Альцгеймера, Паркинсона, Гентингтона и боковой амиотрофический склероз, вызываются общим разрушительным механизмом: накоплением токсичных, неправильно свернутых белков внутри клеток мозга. Поскольку эти «молекулярные двигатели» болезни скрыты за клеточной мембраной, традиционные антитела бессильны против них.
Благодаря этому новому подходу терапия сможет:
— Бить точно в цель: напрямую связываться с вредными белковыми агрегатами именно в месте повреждения;
— Сохранять высокую селективность: отличать здоровые белки от болезненных, неправильно свернутых версий, минимизируя побочные эффекты;
— Использовать доставку генов: будущие методы лечения могут использовать генные технологии, чтобы заставить собственные клетки пациента вырабатывать эти модифицированные фрагменты антител внутри организма.
Глобальное влияние
Хотя нейродегенерация является наиболее приоритетным направлением, потенциальные области применения платформы внутриклеточных антител огромны. В конечном итоге эта технология может быть адаптирована для борьбы с онкологическими заболеваниями, воспалительными расстройствами и редкими генетическими состояниями, где механизм развития болезни локализован внутри клетки.
Этот сдвиг представляет собой фундаментальное изменение биологической стратегии: переход от лечения симптомов на поверхности клетки к воздействию на молекулярные драйверы в самом сердце болезни.
Заключение
Преодолев химические барьеры клеточной среды с помощью инженерных решений под руководством ИИ, ученые открыли новое измерение в разработке лекарств. Этот прорыв превращает антитела из внешних стражей во внутренние прецизионные инструменты, даря надежду на лечение некоторых из самых сложных и разрушительных заболеваний, известных медицине.