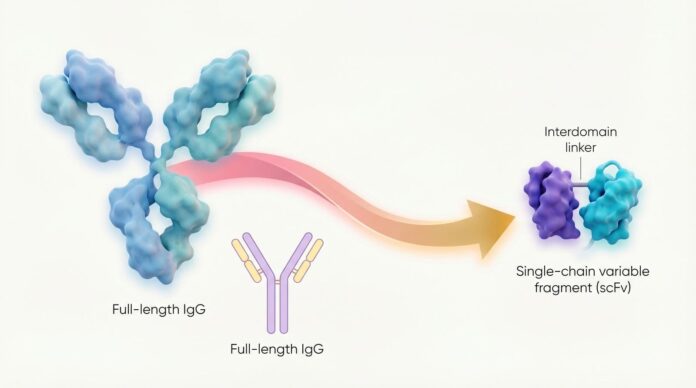
Decennia lang hebben op antilichamen gebaseerde medicijnen gediend als de ruggengraat van de moderne geneeskunde. Hun superkracht ligt in precisie : deze eiwitten zijn ontworpen om specifieke structuren op de oppervlakken van virussen, bacteriën of zieke cellen te herkennen en eraan te binden. Deze precisie is echter altijd met een aanzienlijke beperking gepaard gegaan: antilichamen zijn in wezen ‘externe’ hulpmiddelen. Ze kunnen in de bloedbaan patrouilleren en zich aan de buitenkant van een cel vastklampen, maar historisch gezien zijn ze er niet in geslaagd het celmembraan binnen te dringen om de bedreigingen die daarbinnen op de loer liggen, aan te pakken.
Die barrière begint nu te barsten. Door een combinatie van eiwitreengineering en kunstmatige intelligentie hebben wetenschappers een manier ontwikkeld om de doelgerichte kracht van antilichamen in de cel te brengen.
De uitdaging: waarom cellen vijandig staan tegenover antilichamen
Om te begrijpen waarom dit een doorbraak is, moet je begrijpen waarom eerdere pogingen mislukten. Hoewel onderzoekers lange tijd hebben geprobeerd antilichamen te ‘verkleinen’ tot kleinere fragmenten die theoretisch in cellen zouden kunnen terechtkomen, overleefden deze fragmenten de reis zelden.
Het interieur van een cel is een chemisch verschillende omgeving vergeleken met de bloedbaan. Het voornaamste obstakel is elektrische lading. Standaard antilichaamfragmenten hebben vaak een ladingsprofiel dat, wanneer ze in een cel worden geplaatst, ervoor zorgt dat ze:
– Samenvoeging: De fragmenten plakken aan elkaar in nutteloze klonten.
– Misvouw: Ze verliezen hun functionele vorm.
– Degraderen: Ze gaan kapot voordat ze hun doel kunnen bereiken.
Kortom, het mechanisme dat ze buiten de cel effectief maakt, maakt ze daarbinnen onstabiel.
De oplossing: AI-gestuurd herontwerp
Een nieuwe studie heeft een modulair platform geïntroduceerd om deze stabiliteitscrisis op te lossen. In plaats van te proberen traditionele antilichamen in cellen te forceren, zijn onderzoekers deze van de grond af opnieuw aan het ontwerpen, zodat ze kunnen gedijen in de intracellulaire omgeving.
Door zich te concentreren op het aanpassen van de ladingsverdeling van het doelbindende deel van het antilichaam, hebben wetenschappers met succes meer dan 600 stabiele intracellulaire antilichaamfragmenten gecreëerd.
Hoe het proces werkt:
- Doelbehoud: Het herontwerp richt zich op hoe het antilichaam zich gedraagt in de cel, niet op waar het zich aan bindt. Dit zorgt ervoor dat het medicijn nog steeds zijn specifieke doelwit herkent.
- AI-integratie: Kunstmatige intelligentie wordt gebruikt om eiwitstructuren te modelleren en te wijzigen, waardoor de snelle omzetting van bestaande antilichamen in “intracellulaire” versies mogelijk wordt.
- Schaalbaarheid: Omdat dit een modulair raamwerk is, kan het worden toegepast op honderden bestaande antilichamen, waardoor een enorme bibliotheek met nieuwe therapeutische hulpmiddelen ontstaat.
Een levenslijn voor neurodegeneratieve ziekten
De meest diepgaande implicaties van deze technologie liggen in de behandeling van neurodegeneratieve ziekten.
Aandoeningen zoals de ziekte van Alzheimer, Parkinson, Huntington en motorneuronziekten worden veroorzaakt door een gemeenschappelijk, verwoestend mechanisme: de opeenhoping van giftige, verkeerd gevouwen eiwitten in de cellen van de hersenen. Omdat deze ‘moleculaire motoren’ van ziekten verborgen zijn achter het celmembraan, zijn traditionele antilichamen niet bij machte deze te stoppen.
Met deze nieuwe aanpak kunnen therapieën:
– Richt de bron aan: Bindt zich direct aan schadelijke eiwitaggregaten op de exacte plaats van schade.
– Behoud een hoge selectiviteit: Maak onderscheid tussen gezonde eiwitten en zieke, verkeerd gevouwen versies, waardoor bijwerkingen worden geminimaliseerd.
– Maak gebruik van genafgifte: Toekomstige behandelingen zouden op genen gebaseerde technologieën kunnen gebruiken om de eigen cellen van een patiënt te instrueren om deze opnieuw ontworpen antilichaamfragmenten intern te produceren.
De bredere impact
Hoewel neurodegeneratie de meest directe grens is, zijn de potentiële toepassingen van een intracellulair antilichaamplatform enorm. Deze technologie zou uiteindelijk kunnen worden aangepast voor de behandeling van de kankerbiologie, ontstekingsziekten en zeldzame genetische aandoeningen waarbij het ziekteveroorzakende mechanisme in de cel is gelokaliseerd.
Deze verschuiving vertegenwoordigt een fundamentele verandering in de biologische strategie: van het behandelen van de symptomen op het celoppervlak naar het aanpakken van de moleculaire factoren die de kern van de ziekte vormen.
Conclusie
Door de chemische barrières van het celinterieur te overwinnen door middel van AI-geleide techniek, hebben wetenschappers een nieuwe dimensie van de ontwikkeling van geneesmiddelen ontsloten. Deze doorbraak transformeert antilichamen van externe schildwachten in interne precisie-instrumenten, wat hoop biedt voor de behandeling van enkele van de meest complexe en verwoestende ziekten die de geneeskunde kent.