Pendant des décennies, les médicaments à base d’anticorps ont constitué l’épine dorsale de la médecine moderne. Leur super pouvoir réside dans la précision : ces protéines sont conçues pour reconnaître et se lier à des structures spécifiques à la surface des virus, des bactéries ou des cellules malades. Cependant, cette précision s’est toujours accompagnée d’une limitation importante : les anticorps sont essentiellement des outils « externes ». Ils peuvent patrouiller dans la circulation sanguine et s’accrocher à l’extérieur d’une cellule, mais ils ont toujours été incapables de pénétrer dans la membrane cellulaire pour lutter contre les menaces qui s’y cachent.
Cette barrière commence maintenant à se fissurer. Grâce à une combinaison de réingénierie des protéines et d’intelligence artificielle, les scientifiques ont développé un moyen d’apporter le pouvoir de ciblage des anticorps à l’intérieur de la cellule.
Le défi : pourquoi les cellules sont hostiles aux anticorps
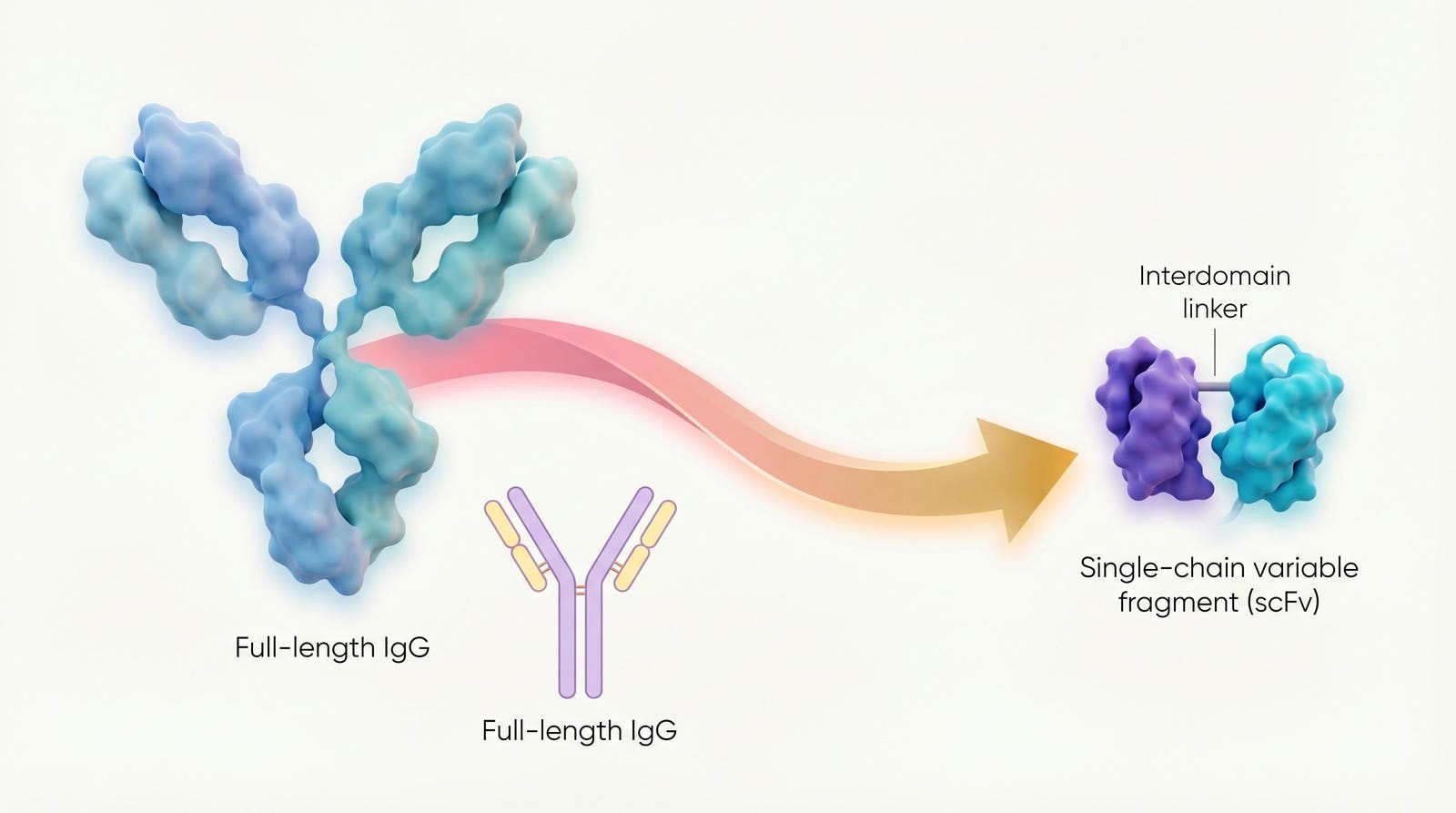
Pour comprendre pourquoi il s’agit d’une avancée majeure, il faut comprendre pourquoi les tentatives précédentes ont échoué. Alors que les chercheurs tentent depuis longtemps de « réduire » les anticorps en fragments plus petits qui pourraient théoriquement se glisser dans les cellules, ces fragments ont rarement survécu au voyage.
L’intérieur d’une cellule est un environnement chimiquement distinct de celui de la circulation sanguine. Le principal obstacle est la charge électrique. Les fragments d’anticorps standards portent souvent un profil de charge qui, lorsqu’ils sont placés à l’intérieur d’une cellule, les amène à :
– Agrégat : Les fragments se collent les uns aux autres en amas inutiles.
– Mal plié : Ils perdent leur forme fonctionnelle.
– Dégrader : Ils s’effondrent avant de pouvoir atteindre leur cible.
En bref, le mécanisme même qui les rend efficaces à l’extérieur de la cellule les rend instables à l’intérieur de celle-ci.
La solution : une refonte basée sur l’IA
Une nouvelle étude a introduit une plateforme modulaire pour résoudre cette crise de stabilité. Plutôt que d’essayer d’introduire de force les anticorps traditionnels dans les cellules, les chercheurs les réorganisent de fond en comble pour prospérer dans l’environnement intracellulaire.
En se concentrant sur l’ajustement de la répartition des charges de la partie de liaison à la cible de l’anticorps, les scientifiques ont réussi à créer plus de 600 fragments d’anticorps intracellulaires stables.
Comment fonctionne le processus :
- Préservation de la cible : La refonte se concentre sur le comportement de l’anticorps à l’intérieur de la cellule, et non sur ce à quoi il se lie. Cela garantit que le médicament reconnaît toujours sa cible spécifique.
- Intégration de l’IA : L’intelligence artificielle est utilisée pour modéliser et modifier les structures protéiques, permettant la conversion rapide des anticorps existants en versions « prêtes pour l’intracellulaire ».
- Évolutivité : Puisqu’il s’agit d’un cadre modulaire, il peut être appliqué à des centaines d’anticorps existants, créant ainsi une bibliothèque massive de nouveaux outils thérapeutiques.
Une bouée de sauvetage pour les maladies neurodégénératives
Les implications les plus profondes de cette technologie résident dans le traitement des maladies neurodégénératives.
Des maladies telles que la maladie d’Alzheimer, la maladie de Parkinson, la maladie de Huntington et la maladie des motoneurones sont provoquées par un mécanisme commun et dévastateur : l’accumulation de protéines toxiques et mal repliées à l’intérieur des cellules du cerveau. Parce que ces « moteurs moléculaires » de la maladie sont cachés derrière la membrane cellulaire, les anticorps traditionnels sont impuissants à les arrêter.
Avec cette nouvelle approche, les thérapies peuvent :
– Ciblez la source : Se lie directement aux agrégats de protéines nocives sur le site exact du dommage.
– Maintenir une sélectivité élevée : Faites la distinction entre les protéines saines et les versions malades et mal repliées, minimisant ainsi les effets secondaires.
– Tirer parti de la délivrance de gènes : Les futurs traitements pourraient utiliser des technologies basées sur les gènes pour demander aux propres cellules d’un patient de produire en interne ces fragments d’anticorps redessinés.
L’impact plus large
Même si la neurodégénérescence constitue la frontière la plus immédiate, les applications potentielles d’une plateforme d’anticorps intracellulaires sont vastes. Cette technologie pourrait éventuellement être adaptée pour traiter la biologie du cancer, les troubles inflammatoires et les maladies génétiques rares où le mécanisme à l’origine de la maladie est localisé dans la cellule.
Ce changement représente un changement fondamental dans la stratégie biologique : passer du traitement des symptômes à la surface des cellules à la lutte contre les moteurs moléculaires au cœur de la maladie.
Conclusion
En surmontant les barrières chimiques de l’intérieur des cellules grâce à une ingénierie guidée par l’IA, les scientifiques ont ouvert une nouvelle dimension du développement de médicaments. Cette avancée transforme les anticorps des sentinelles externes en outils internes de précision, offrant ainsi l’espoir de traiter certaines des maladies les plus complexes et les plus dévastatrices connues de la médecine.